Teknik seni digital sekarang dapat merancang biomolekul kustom yang berfungsi sesuai permintaan.
“OK. Mari kita mulai.” David Juergens, seorang ahli kimia komputasi di University of Washington (UW) di Seattle, akan merancang protein yang dalam lebih dari 3 miliar tahun percobaan evolusi belum pernah diproduksi.
Dalam panggilan video, Juergens membuka versi berbasis awan dari alat kecerdasan buatan (AI) yang ia bantu kembangkan, yang disebut RFdiffusion. Jaringan saraf ini, dan yang lainnya seperti itu, membantu menghadirkan penciptaan protein kustom – yang sebelumnya merupakan usaha yang sangat teknis dan seringkali tidak berhasil – ke dalam ilmu utama.
Protein-protein ini dapat membentuk dasar untuk vaksin, terapi, dan biomaterial. “Ini adalah momen yang benar-benar transformatif,” kata Gevorg Grigoryan, salah satu pendiri dan kepala teknis Generate Biomedicines di Somerville, Massachusetts, sebuah perusahaan bioteknologi yang menerapkan desain protein untuk pengembangan obat.
Alat-alat ini terinspirasi oleh perangkat lunak AI yang mensintesis gambar realistis, seperti perangkat lunak Midjourney yang pada tahun ini terkenal digunakan untuk menghasilkan gambar viral Paus Fransiskus mengenakan jaket puffer putih desainer. Pendekatan konseptual serupa, para peneliti telah menemukan, dapat menghasilkan bentuk protein yang realistis sesuai dengan kriteria yang ditentukan oleh desainer – artinya, misalnya, bahwa memungkinkan untuk dengan cepat merancang protein baru yang harus terikat erat dengan biomolekul lain. Dan eksperimen awal menunjukkan bahwa ketika para peneliti memproduksi protein-protein ini, sebagian yang berguna dapat berfungsi seperti yang diusulkan oleh perangkat lunak.
Para peneliti mengatakan bahwa alat-alat ini telah merevolusi proses merancang protein dalam setahun terakhir. “Ini adalah ledakan dalam kemampuan,” kata Mohammed AlQuraishi, seorang ahli biologi komputasi di Columbia University di New York City, yang timnya telah mengembangkan salah satu alat seperti itu untuk desain protein. “Anda sekarang dapat membuat desain dengan kualitas yang diinginkan.”
“Anda sedang membangun struktur protein yang disesuaikan untuk masalah tertentu,” kata David Baker, seorang biofisikawan komputasi di UW yang kelompoknya, termasuk Juergens, mengembangkan RFdiffusion. Tim merilis perangkat lunak pada Maret 2023, dan sebuah makalah yang menjelaskan jaringan saraf tersebut muncul minggu ini di Nature 1. (Versi pra-cetak dirilis pada akhir 2022, pada saat yang sama ketika beberapa tim lain, termasuk AlQuraishi 2 dan Grigoryan 3, melaporkan jaringan saraf serupa).
Untuk pertama kalinya, para perancang protein sekarang memiliki alat-alat reproduktif dan tangguh di sekitar mana industri baru dapat diciptakan, tambah Grigoryan. “Tantangan selanjutnya adalah apa yang akan Anda lakukan dengannya?”
Desain besar
Juergens memasukkan beberapa spesifikasi untuk protein yang diinginkannya ke dalam formulir web yang menyerupai kalkulator pajak online. Ini harus memiliki panjang 100 asam amino dan membentuk kompleks dua protein simetris yang disebut homodimer. Banyak reseptor sel mengadopsi konfigurasi ini, dan homodimer baru dapat menjadi molekul sinyal sel sintetis, kata Joe Watson, seorang bio-kimia komputasi UW yang juga turut mengembangkan RFdiffusion, dan juga berada dalam panggilan video. Tetapi desain pagi ini tidak dimaksudkan untuk melakukan apa pun kecuali menyerupai protein yang realistis.
Para peneliti telah berjuang selama beberapa dekade untuk membangun protein baru. Pada awalnya, mereka mencoba untuk menyusun bagian-bagian berguna dari protein-protein yang sudah ada, seperti kantong enzim di mana reaksi kimia dicatalisis. Pendekatan ini bergantung pada pemahaman tentang bagaimana protein melipat dan bekerja, serta intuisi dan banyak percobaan. Para ilmuwan kadang-kadang menyaring ribuan desain untuk mengidentifikasi satu yang berhasil seperti yang diharapkan.
Moment cahaya datang dengan AlphaFold (dikembangkan oleh perusahaan AI berbasis London DeepMind, sekarang Google DeepMind) dan model berbasis AI lainnya yang dapat memprediksi struktur protein dengan akurat dari urutan asam amino, kata Baker. Para perancang menyadari bahwa jaringan saraf ini, dilatih pada urutan dan struktur protein nyata, juga dapat membantu menciptakan protein dari awal.
Dalam beberapa tahun terakhir, tim Baker dan orang lain di bidang ini telah merilis sejumlah alat desain protein berbasis AI. Salah satu pendekatan yang digunakan oleh alat-alat ini, yang disebut halusinasi, melibatkan menciptakan urutan asam amino acak yang kemudian dioptimalkan oleh AlphaFold, atau alat serupa yang disebut RoseTTAFold, hingga menyerupai sesuatu yang jaringan saraf menyarankan mampu melipat menjadi struktur tertentu. Pendekatan lain, yang disebut inpainting, mengambil potongan tertentu dari urutan atau struktur protein dan membangun sisa molekul di sekitarnya menggunakan RoseTTAFold.
Namun, alat-alat ini jauh dari sempurna. Percobaan cenderung menunjukkan bahwa struktur yang dirancang dengan metode halusinasi tidak selalu membentuk protein yang terlipat dengan baik ketika dibuat di laboratorium, dan akhirnya berakhir sebagai lumpur di dasar tabung tes, misalnya. Metode halusinasi juga kesulitan membuat protein yang lebih besar selain protein kecil (meskipun peneliti lain menunjukkan, dalam prapublikasi Februari, bagaimana teknik ini dapat digunakan untuk merancang molekul yang lebih panjang). Inpainting juga kurang berhasil dalam membentuk protein ketika diberi potongan yang lebih pendek. Bahkan ketika pendekatan itu menghasilkan struktur protein teoretis, ia tidak dapat menghasilkan solusi yang beragam untuk masalah yang akan meningkatkan peluang keberhasilan.
Di sinilah RFdiffusion dan AI desain protein serupa, yang dirilis dalam beberapa bulan terakhir, masuk. Mereka didasarkan pada prinsip yang sama dengan jaringan saraf yang menghasilkan gambar realistis, seperti Stable Diffusion, DALL-E, dan Midjourney. Jaringan ‘diffusi’ ini dilatih pada data, baik itu gambar atau struktur protein, yang kemudian semakin bising, akhirnya tidak menyerupai gambar atau struktur awal. Jaringan kemudian belajar untuk ‘membersihkan’ data, melakukan tugas secara terbalik.
Jaringan seperti RFdiffusion dilatih pada puluhan ribu struktur protein nyata yang disimpan dalam repositori yang disebut Bank Data Protein (PDB). Ketika jaringan membuat protein baru, ia dimulai dengan total kebisingan: kumpulan asam amino acak. “Anda bertanya apa protein yang menyebabkan kebisingan,” jelas Watson. Setelah beberapa putaran membersihkan, ia menghasilkan sesuatu yang menyerupai protein nyata — tetapi baru.
Ketika tim Baker menguji RFdiffusion tanpa memberikan panduan kecuali panjang protein, jaringan menghasilkan protein yang berbeda-beda dan realistis, berbeda dari apa pun yang dilatih di PDB. Namun, para peneliti juga dapat mengarahkan program untuk membuat protein sesuai dengan kendala desain tertentu selama proses membersihkan, proses yang disebut kondisioning.
Misalnya, tim Baker mengkondisikan RFdiffusion untuk membuat protein yang termasuk lipatan tertentu, atau dapat bersarang di permukaan molekul lain (interaksi yang mendasari pengikatan). Tim Grigoryan bahkan mengembangkan jaringan difusi yang disebut Chroma dan kemudian mengkondisikannya untuk membuat protein yang berbentuk seperti 26 huruf kapital yang digunakan dalam bahasa Inggris, serta angka Arab.
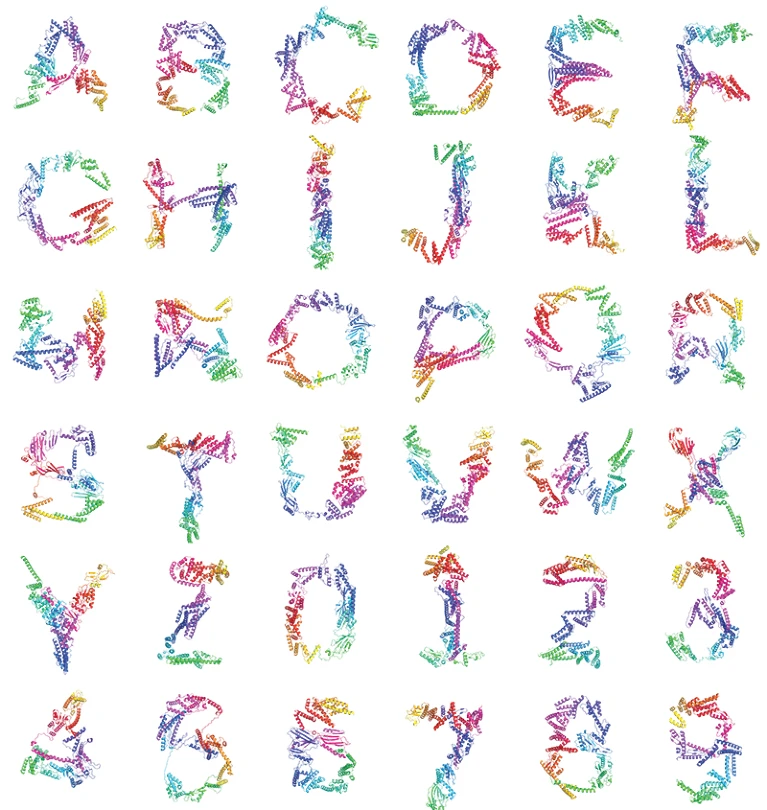
Sinyal dari Noise
Layar komputer Juergens awalnya menunjukkan noise, yaitu kumpulan asam amino acak yang dimulai oleh sistem AI. Mereka direpresentasikan sebagai coretan merah yang samar-samar menyerupai lukisan jari anak kecil. Mereka berubah, frame by frame, menjadi bentuk yang semakin kompleks, dengan fitur seperti spiral ketat yang dikenal sebagai α-heliks dan bentuk pita yang melengkung kembali pada dirinya sendiri, disebut β-lembaran. “Ini adalah topologi alpha-beta yang bagus,” kata Juergens, sambil tersenyum ketika ia mengagumi karya yang hanya memakan waktu beberapa menit untuk dibuat. “Ini terlihat bagus.”
Alat ini telah banyak digunakan di laboratorium Baker. “Proses desain hampir tidak dikenali dibandingkan dengan satu tahun yang lalu,” katanya. Jaringan saraf telah unggul dalam tantangan desain yang tidak efisien, sulit atau tidak mungkin dilakukan dengan pendekatan lain.
Dalam satu analisis yang dilaporkan dalam studi mereka, para peneliti memulai dengan potongan dari protein lain, seperti bagian dari protein virus yang dikenali oleh sel-sel kekebalan, dan memberikan tugas pada alat berbasis AI untuk menghasilkan 100 protein baru yang berbeda, untuk melihat berapa banyak yang akan menggabungkan motif yang diinginkan. Tim melakukan tantangan ini untuk 25 bentuk awal yang berbeda. Hasilnya tidak selalu menggabungkan potongan awal, tetapi RFdiffusion menghasilkan setidaknya satu protein yang melakukannya untuk 23 motif, dibandingkan dengan 15 untuk halusinasi dan 12 untuk inpainting.
RFdiffusion juga terbukti mahir dalam membuat protein yang dapat dirakit sendiri menjadi nanopartikel kompleks yang mungkin dapat mengirimkan obat-obatan atau komponen vaksin. Pendekatan kecerdasan buatan sebelumnya juga dapat membuat jenis protein ini, tetapi Watson mengatakan desain RFdiffusion jauh lebih canggih.
Jaringan saraf seperti RFdiffusion tampaknya sangat berbakat saat ditugaskan untuk merancang protein yang dapat melekat pada protein lain yang ditentukan. Tim Baker telah menggunakan jaringan untuk membuat protein yang terikat kuat pada protein yang terlibat dalam kanker, penyakit autoimun, dan kondisi lainnya. Salah satu keberhasilan yang belum dipublikasikan, katanya, adalah merancang pengikat kuat untuk molekul sinyal imun yang sulit diincar yang disebut reseptor faktor nekrosis tumor – target untuk obat antibodi yang menghasilkan miliaran dolar pendapatan setiap tahun. “Ini memperluas ruang protein yang dapat kami buat pengikatnya dan membuat terapi yang bermakna,” kata Watson.
Pengujian dunia nyata
Tim Baker menghasilkan begitu banyak desain sehingga menguji apakah mereka bekerja seperti yang dimaksudkan telah menjadi bottleneck serius. “Satu orang yang ahli dalam pembelajaran mesin dapat menghasilkan cukup banyak desain untuk membuat 100 ahli biologi sibuk selama berbulan-bulan,” kata Kevin Yang, seorang peneliti pembelajaran mesin biomedis di Microsoft Research di Cambridge, Massachusetts, yang timnya telah mengembangkan alat desain protein berbasis difusi mereka sendiri.
Tetapi tanda-tanda awal menunjukkan bahwa kreasi RFdiffusion adalah hal yang nyata. Dalam tantangan lain yang dijelaskan dalam studi mereka, tim Baker menugaskan alat itu untuk merancang protein yang mengandung rangkaian kunci p53, molekul sinyal yang overaktif dalam banyak kanker (dan target obat yang dicari). Ketika para peneliti membuat 95 desain perangkat lunak itu (dengan merekayasa bakteri untuk mengekspresikan protein), lebih dari setengahnya mempertahankan kemampuan p53 untuk melekat pada target alaminya, MDM2. Desain terbaik melakukannya sekitar 1.000 kali lebih kuat daripada p53 alami. Ketika para peneliti mencoba tugas ini dengan halusinasi, desainnya – meskipun diprediksi akan berhasil – tidak berhasil di tabung reaksi, kata Watson.
Secara keseluruhan, Baker mengatakan timnya telah menemukan bahwa 10-20% desain RFdiffusion melekat pada target yang dimaksudkan dengan cukup kuat untuk berguna, dibandingkan dengan kurang dari 1% untuk metode sebelumnya sebelum kecerdasan buatan. (Pendekatan pembelajaran mesin sebelumnya tidak dapat merancang pengikat secara andal, kata Watson). Ahli biokimia Matthias Gloegl, seorang rekan di UW, mengatakan bahwa akhir-akhir ini ia telah mencapai tingkat keberhasilan mendekati 50%, yang berarti hanya perlu seminggu atau dua untuk menghasilkan desain kerja, dibandingkan dengan berbulan-bulan. “Ini benar-benar gila,” katanya.
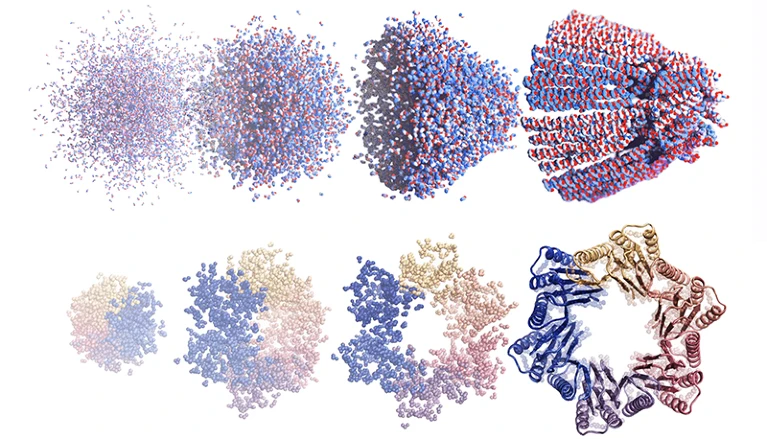
Sebuah perakitan protein berbentuk corong (atas) dan struktur berbentuk cincin dengan enam rantai protein (bawah), dirancang dari kebisingan menggunakan generator seni AI berbasis difusi. Kredit: Ian C. Haydon / Institut Desain Protein UW
Versi berbasis awan dari RFdiffusion memiliki sekitar 100 pengguna setiap hari pada akhir Juni, menurut Sergey Ovchinnikov, seorang ahli biologi evolusi di Universitas Harvard di Cambridge, Massachusetts. Joel Mackay, seorang biokimiawan di Universitas Sydney di Australia, telah mencoba RFdiffusion untuk mendesain protein yang mampu mengikat protein lain yang diteliti oleh laboratoriumnya, termasuk molekul yang disebut faktor transkripsi yang mengontrol aktivitas gen dalam sel. Dia menemukan proses desain sederhana, dan menggunakan pemodelan komputer untuk memvalidasi bahwa, secara teori, protein harus dapat mengikat faktor transkripsi.
Mackay sekarang sedang menguji apakah protein dapat mengubah ekspresi gen seperti yang dimaksud ketika diproduksi dalam sel. Dia berharap, karena temuan seperti itu akan menjadi cara sederhana untuk mengaktifkan dan menonaktifkan faktor transkripsi tertentu dalam sel, bukan menggunakan obat yang bisa memakan waktu bertahun-tahun untuk diidentifikasi, jika dapat ditemukan sama sekali. “Jika metode ini bekerja dengan andal untuk jenis protein kami, itu akan menjadi perubahan permainan total,” katanya.
Peningkatan di masa depan
Model terbaru seperti RFdiffusion adalah “perubahan langkah” kata Charlotte Deane, seorang informatician imun di Universitas Oxford, Inggris. Namun tantangan utama masih ada. “Apa yang akan dilakukannya adalah menginspirasi orang untuk melihat sejauh mana kita bisa mendorong metode difusi ini,” katanya.
Salah satu aplikasi yang dia dan ilmuwan lain serta perusahaan bioteknologi sangat tertarik adalah merancang protein pengikat yang lebih kompleks seperti antibodi, atau reseptor protein yang digunakan oleh sel T (jenis sel kekebalan). Protein-protein ini memiliki loop fleksibel yang saling mengunci dengan target mereka, dibandingkan dengan antarmuka datar seperti sandwich yang RFdiffusion telah berhasil sejauh ini. Baker mengatakan mereka membuat kemajuan dengan antibodi.
Ovchinnikov dan yang lain mengatakan sulit secara umum untuk merancang biomolekul yang fungsinya bergantung pada wilayah yang lembut sehingga memberi mereka kemampuan untuk mengadopsi banyak bentuk yang berbeda. Ini adalah fitur yang sulit dimodelkan menggunakan AI. “Jika masalahnya adalah, dapatkah kita terikat pada sesuatu dan menghambatnya,” kata Ovchinnikov, “Saya pikir masalah itu akan terselesaikan dengan metode ini. Tetapi untuk melakukan sesuatu yang lebih kompleks, lebih seperti apa yang dilakukan alam, Anda perlu memperkenalkan beberapa fleksibilitas.”
Tanja Kortemme, seorang biolog komputasi di Universitas California, San Francisco, menggunakan RFdiffusion untuk merancang protein yang dapat digunakan sebagai sensor atau sebagai saklar untuk mengontrol sel. Dia mengatakan bahwa jika situs aktif protein bergantung pada penempatan beberapa asam amino, jaringan AI berhasil, tetapi sulit untuk merancang protein dengan situs aktif yang lebih kompleks, memerlukan banyak asam amino kunci lainnya – tantangan yang sedang dihadapi oleh dia dan rekan-rekannya.
Salah satu keterbatasan metode difusi terbaru adalah ketidakmampuannya untuk menciptakan protein yang sangat berbeda dari protein alami, kata Yang. Hal itu karena sistem AI hanya dilatih pada protein yang sudah ada yang telah dikarakterisasi oleh ilmuwan, dan cenderung menciptakan protein yang menyerupai itu. Menciptakan protein yang terlihat lebih asing mungkin memerlukan pemahaman yang lebih baik tentang fisika yang memberikan fungsi pada protein.
Ini dapat memudahkan desain protein untuk menjalankan tugas yang tidak pernah dilakukan oleh protein alami. “Masih ada banyak ruang untuk berkembang,” kata Yang.
Alat desain protein terbaru terbukti sangat kuat dalam menciptakan protein yang dapat melakukan tugas tertentu – selama fungsi itu dapat dijelaskan dalam hal bentuk, seperti permukaan protein untuk mengikat, kata AlQuraishi. Namun, katanya, alat seperti RFdiffusion belum mampu menangani jenis spesifikasi lain, seperti membuat protein yang dapat melakukan reaksi tertentu tanpa memperhatikan bentuknya – ketika “Anda tahu apa yang Anda inginkan tetapi Anda tidak tahu geometrinya”.
Alat desain protein masa depan juga akan membutuhkan kemampuan untuk menghasilkan protein dengan berbagai kriteria yang berbeda, kata Grigoryan. Sebuah protein terapeutik potensial tidak hanya harus dapat mengikat targetnya, tetapi juga tidak boleh mengikat yang lain dan harus memiliki sifat-sifat yang memudahkan produksi massal.
Salah satu arah penelitian yang sedang dieksplorasi oleh para peneliti adalah apakah protein dapat dirancang menggunakan deskripsi teks sederhana, mirip dengan instruksi yang diberikan kepada alat generasi gambar seperti Midjourney. “Anda benar-benar bisa membayangkan bahwa kita akan dapat menulis deskripsi protein dan membuatnya disintesis dan diuji,” kata Watson.
Grigoryan dan rekan-rekannya telah mengambil langkah menuju tujuan ini. Dalam pra-cetakannya pada Desember 2022, mereka melatih Chroma untuk menempelkan deskripsi pada desainnya dan mengeluarkan desain sesuai dengan spesifikasi berbasis teks, termasuk “protein dengan domain CHAD” (bentuk protein yang menggabungkan beberapa heliks) atau “struktur kristal aminotransferase” (enzim yang terlibat dalam pembuatan dan pemecahan protein).
Protein yang dibuat oleh Juergens dalam beberapa menit pagi ini hanya merupakan model struktur 3D protein. Juergens kemudian menggunakan alat AI lain untuk menciptakan urutan asam amino yang harus dilipat menjadi struktur tersebut. Sebagai pemeriksaan terakhir, ia memasukkan urutan tersebut ke AlphaFold untuk melihat apakah perangkat lunak tersebut memprediksi struktur lipatan yang sesuai dengan desain. Mereka tepat sekali, dengan prediksi AlphaFold berbeda dari desain rata-rata hanya sebesar 1 ångström (lebar atom hidrogen).
“Ini adalah akurasi yang kami anggap sebagai keberhasilan desain,” kata Watson. Satu-satunya hal yang perlu dilakukan, katanya, adalah melihat bagaimana performa protein tersebut di kehidupan nyata.
Leave a Reply